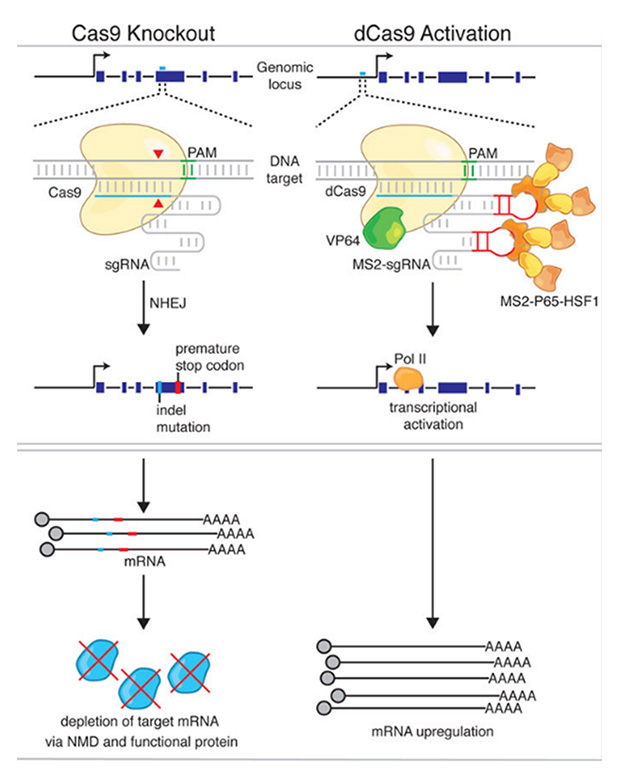
CRISPR/Cas9系统是一种原核生物的免疫系统,是细菌用来抵抗病毒和外源质粒入侵的一种防御机制。目前最成熟且应用最广的是Type II的CRISPR/Cas9系统,其原理是利用gRNA特异性识别靶序列,并引导Cas9核酸内切酶结合到DNA的靶序区域。当Cas9核酸内切酶为野生型的,其会在该靶序区域的PAM上游进行切割,从而造成靶位点DNA双链断裂,随之利用细胞的非同源末端连接(NHEJ)或同源重组(HDR)的方式对切割位点进行修复,实现DNA水平的敲除、敲入或点突变。当Cas9核酸内切酶为突变型的,其无法在该靶序区域的PAM上游进行切割,只会结合在该区域,起到定位与之偶联蛋白的作用,再通过这些偶联蛋白发挥功能,实现干扰或过表达目的基因的效果。
慢病毒(Lentivirus)包装所用载体是以 HIV-1 (人类免疫缺陷1型病毒)为基础,使用疱疹病毒VSVG 外壳蛋白发展起来的工具载体。由于其毒性基因已经被剔除并被外源性目的基因所取代,且不具有自我增殖的能力,属于假型病毒。慢病毒具有感染谱广泛特点,并且可以有效感染分裂和非分裂细胞。侵染宿主细胞后,慢病毒利用反转录酶将其RNA转录成双链DNA,随后永久的整合到宿主细胞的染色体中,实现长时间稳定表达。 此外,慢病毒免疫原性低,不易造成免疫反应,所以现在慢病毒系统除了被广泛应用到各种细胞系、活体动物实验中。
利用慢病毒载体大规模导入全基因组sgRNA文库,能够同时靶向数千个基因,实现高通量的功能基因筛选。
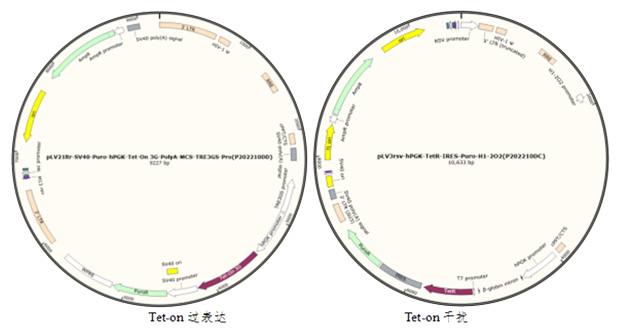
Tet-on慢病毒
Tet调控基因表达系统是以大肠杆菌Tn10转座子上Tet抗性操纵子为基础而建立的。Tet阻遏蛋白(Tet repressor protein, TetR)与Tet操纵子(Tet operator, TetO)能够特异性结合。当细胞内无Tet存在时,Tet会与TetO结合,从而阻断下游抗性基因表达;当有Tet存在时,Tet使TetR构象发生改变,导致TetR与TetO分离,使下游抗性基因得以表达,细菌从而获得耐药性。
慢病毒(Lentivirus)包装所用载体是以 HIV-1 (人类免疫缺陷1型病毒)为基础,使用疱疹病毒VSVG 外壳蛋白发展起来的工具载体。由于其毒性基因已经被剔除并被外源性目的基因所取代,且不具有自我增殖的能力,属于假型病毒。慢病毒具有感染谱广泛特点,并且可以有效感染分裂和非分裂细胞。侵染宿主细胞后,慢病毒利用反转录酶将其RNA转录成双链DNA,随后永久的整合到宿主细胞的染色体中,实现长时间稳定表达。 此外,慢病毒免疫原性低,不易造成免疫反应,所以现在慢病毒系统除了被广泛应用到各种细胞系、活体动物实验中。
Tet-on慢病毒通过慢病毒将Tet-on过表达/干扰系统所需要的元件整合到目的细胞中,实现高效率、精准、安全、可逆性的调控。
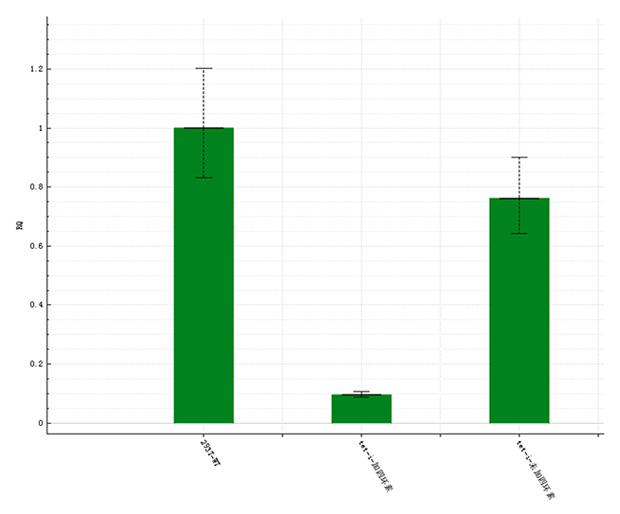
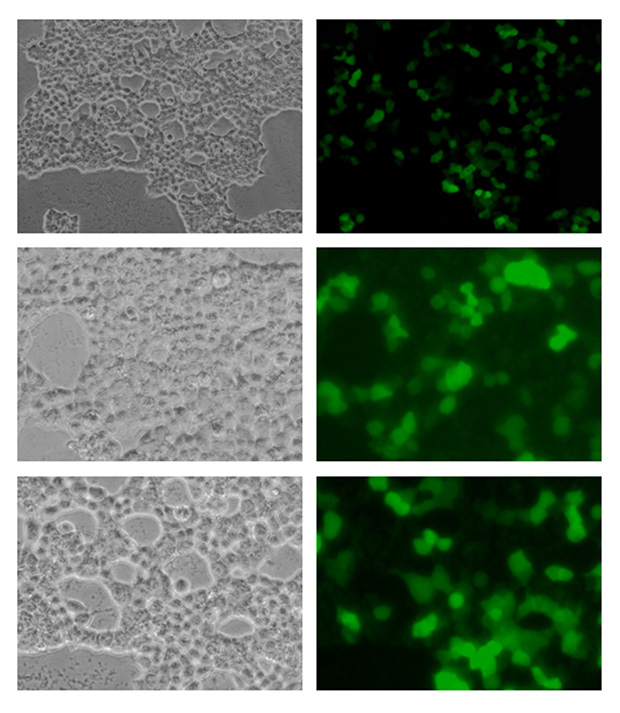
Tet-on 过表达GFP测试结果
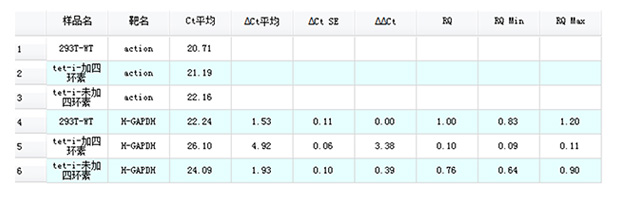
病毒侵染293T后,未加四环素的情况下,细胞照片如下:

未进行Puro药杀,添加四环素(终浓度10ug/mL)后,大约48H后的结果如下:
Tet-on 干扰GAPDH测试结果